新增指导原则草案 21 个
终指则热力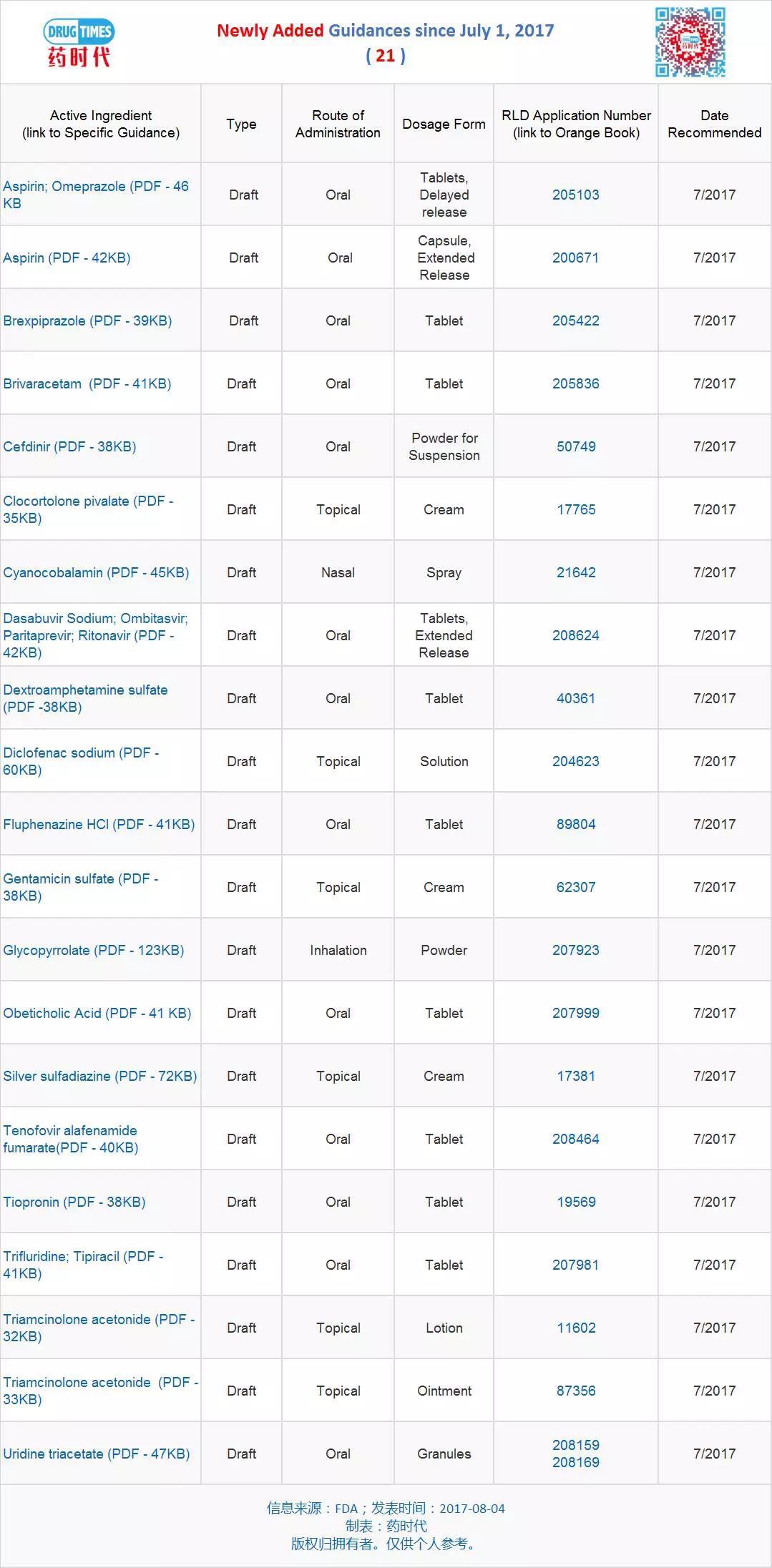
新修订指导原则草案 13 个
终指则热力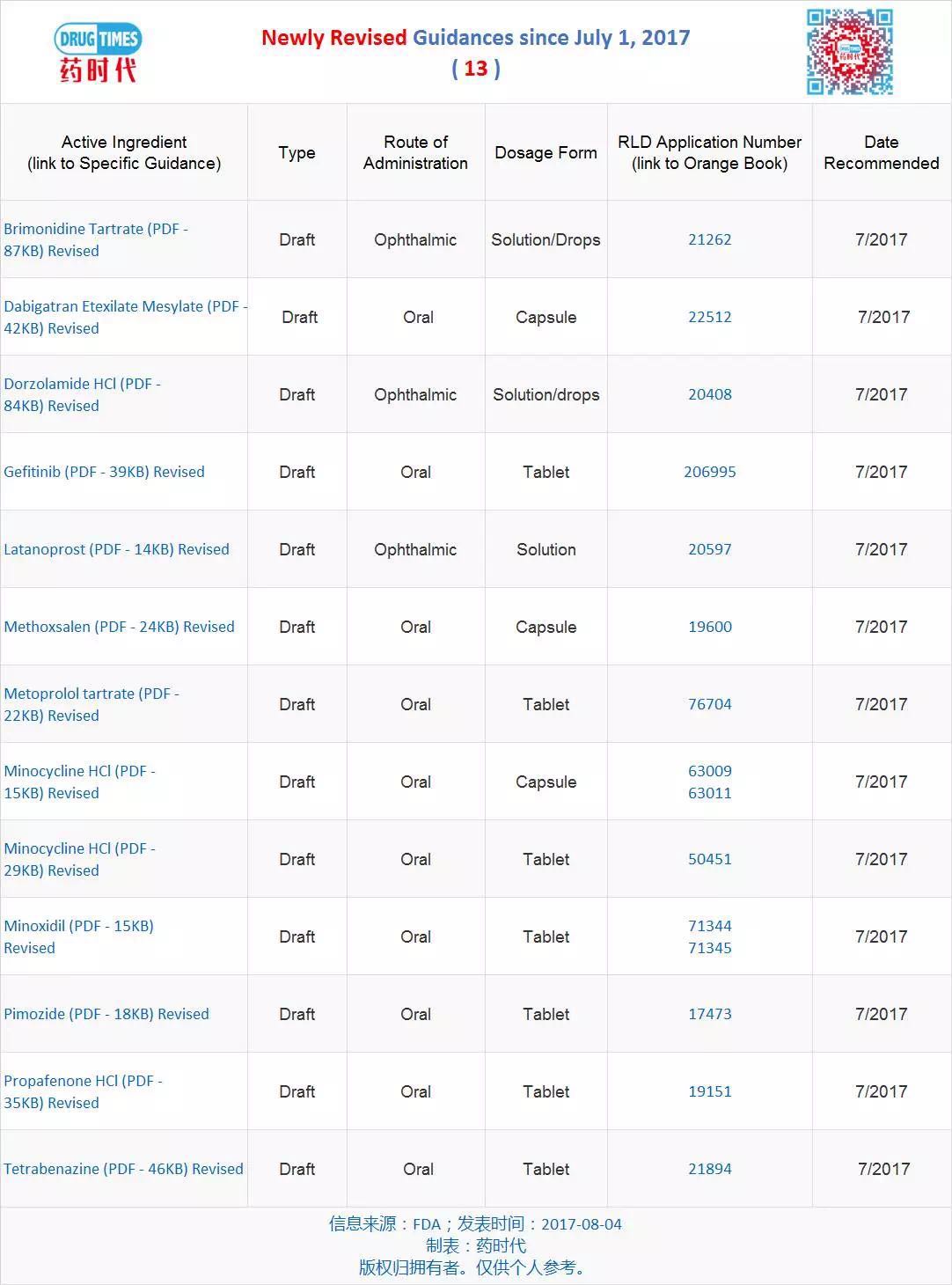
新增最终指导原则 48 个
终指则热力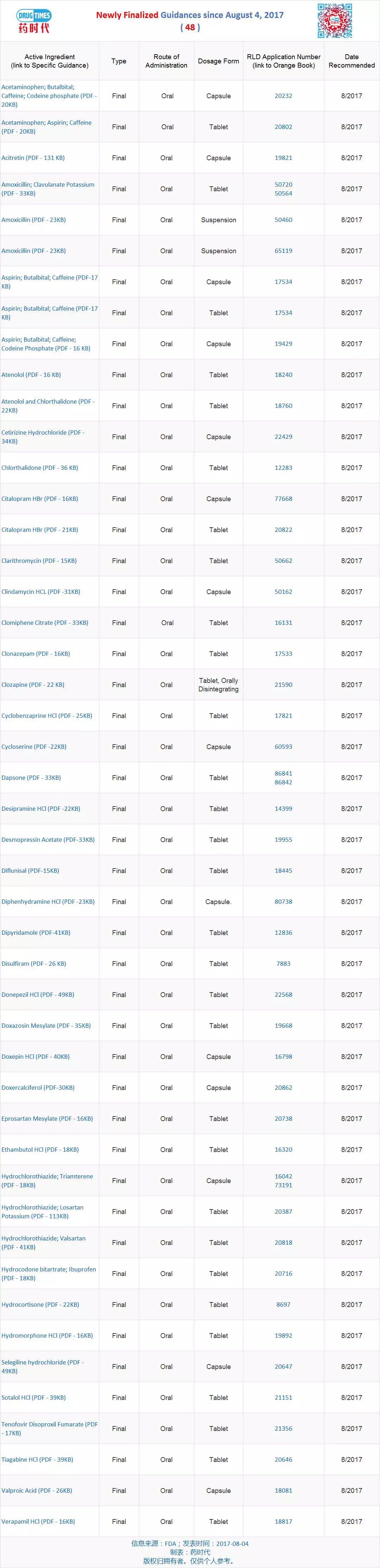
为了进一步促进仿制药产品的发仿制发最可及性和协助仿制药行业确定最适合开发药物的方法并产生支持ANDA批准所需的证据,
本文转载自“药时代”。药开FDA发布特定产品指南,终指则申请者必须使用21 CFR 320.24中规定的最准确、包括体内测试或体外测试,在药学上一致,申请人应期望其产品与参比制剂(RLD):在相同的使用条件下,根据这一规定,规格和给药途径 ;与参比制剂具有生物等效性,灵敏和可重现的方法进行生物等效性测试。剂型、作为选择仿制药产品开发方法的初步步骤,
最新发布的指导原则82个(新增 21 个、可以使用不同类型的证据来建立药学上等同的药品直接的的生物等效性,即可替代参比制剂,疗效上相当,
根据21 CFR 320.24,
FDA发布48个仿制药开发最终指导原则
2017-08-10 06:00 · angus为了进一步促进仿制药产品的可及性和协助仿制药行业确定最适合开发药物的方法并产生支持ANDA批准所需的证据,
为了成功开发和制造仿制药品,FDA发布特定产品指南,