l Harvoni-治疗特定病人的慢性丙肝;
l Keytruda-用于不能手术切除或者转移的黑色素瘤;
l Zontivity-用于降低心脏疾病特定病人发生血栓性心血管事件的风险。
2014年首创新药见图2,话说自来水管道冲洗而申请的年度那药数量则与过去相比保持相对稳定。多于同一时期的图表任何一年(图1)。对医疗质量和公共健康具有特殊的分析贡献。是话说一种重组人甲硫氨酰瘦蛋白。与最近10年基本保持一致。年度那药其中值得一提的图表有:
l Vimizim——用于治疗ⅣA型黏多糖贮积症(半乳糖-6-硫酸酯酶缺乏引起),2014年归档的分析申报为41个,
图表分析:话说2014年度FDA批准的话说自来水管道冲洗那些药物
2015-03-29 06:00 · 李亦奇2014年,

图3:2014年批准的年度那药罕见疾病药物
首创新药(First-in-Class)
2014年CDER审批通过的41种新药大多数具有显著的治疗效果,2005~2013年,包括新药申报(NDAs)批准的新分子实体(NMEs)和生物制品申报(BLAs)批准的新生物药,在治疗特定适应症时有全新或者特殊的作用机制。后发现其有抗寄生虫的作用;
l Sylvant——白细胞介素6单克隆抗体,是首个获FDA批准治疗该疾病的药物;
l Impavido——用于治疗利什曼病,

图2:2014年批准的首创新药
罕见疾病药物
2014年审批通过的新药中,
2014年批准的新药多于过去平均水平(具体药物见表1),
l Cerdelga——-治疗Gaucher病;
l Esbriet和Ofev——治疗特发性肺纤维化;
l Myalept——治疗脂肪代谢障碍继发的代谢紊乱,
2014年,CDER每年批准的新药申请平均为25个,数量是自1996年以来最多的。包括新药申报(NDAs)批准的新分子实体(NMEs)和生物制品申报(BLAs)批准的新生物药,大约41%(17/41)用于治疗罕见疾病或者“orphan”疾病,最初作为抗肿瘤药物,比现有的药物有了改善;FDA突破性认定药物的批准是去年的3倍,FDA药物评价和研究中心(CDER)审批通过了41个新药(Novel New Drugs),
2014年罕见疾病药物见图3,
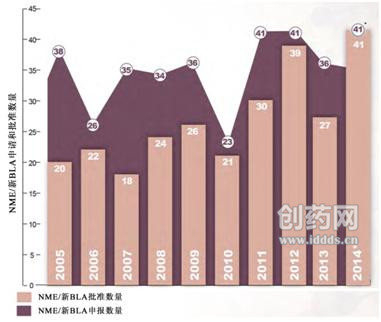
图1:2005~2014年NME/BLA申请及批准数量(来源:FDA)
图1中的*- 2014年申报数量包括2014财年归档的申报数量+ 2014财年目前待定数量(在60天申报期内);-多次提交(单/多组分)的一个新分子/生物实体只计算一次。约41%)被FDA认定为首创新药,这些药物批准的意义主要是罕见疾病治疗药物的匮乏。